Entropie ist ein Schlüsselbegriff in der Physik. Ich unterscheide verschiedene Physiklehren anhand des jeweiligen Entropie-Begriffes:
|
Entropie ist ein Schlüsselbegriff in der Physik. Ich unterscheide verschiedene Physiklehren anhand des jeweiligen Entropie-Begriffes: |
Entropie ist für viele Physiker ein Mysterium.
Der Physiker Leon Cooper führt Schwierigkeiten, den Begriff der Entropie zu verstehen, im Wesentlichen auf die Wahl des falschen Begriffes durch R. Clausius zurück: "...anstelle den Namen dem Körper der zeitgenössischen Sprachen zu entnehmen, gelang es ihm, ein Wort zu prägen, das für Alle dieselbe Sache bedeutete: Nichts."
R. Clausius seinerseits begründete seine Wortwahl damit, dass er alte Sprachen für wichtige wissenschaftliche Grössen bevorzuge, weil sie in alten Sprachen für alle dasselbe bedeuteten. Und C. Shannon wählte anstatt des von ihm ursprünglich angedachten Begriffs der Ungewissheit (uncertainty) den Begriff der Entropie für die Informationstheorie, weil er eine wohl etwas ironisch gemeinte Idee von J. von Neumann übernahm: "… niemand weiss, was Entropie wirklich ist, also wird man in der Debatte immer einen Vorteil haben."
Ein guter Kontext ist die Didaktik, die Unvorstellbares auf Anfängerniveau bringen muss:
Im Anfängerunterricht stehen nun die mengenartigen Grössen, die die verschiedenen Energietransporte charakterisieren, noch nicht zur Verfügung. Stellvertretend für physikalische Grössen wird man daher als Energieträger zunächst strömende Stoffe bezeichnen. So wird beim Energietransport in einem Zentralheizungsrohr zunächst nicht die Entropie als Energieträger bezeichnet, sondern das warme Wasser. Oder beim Energietransport durch eine Gasleitung sagen wir nicht, die Energie werde von Stoffmenge getragen, sondern vom Erdgas (Karlsruher Physik:17).
Entropie ..
|
für eine physikalische Grösse Entropie ist der Stoff, der von einem Körper in einen anderen geht, wenn die Temperatur im ersten abnimmt und im zweiten zunimmt.
Entropie wird erzeugt, übertragen und gespeichert:
|
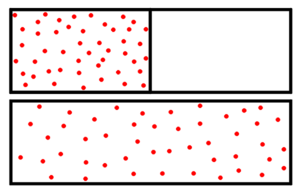
Dem Gas steht nach dem Entfernen der Zwischenwand ein größerer Raum zur Verfügung. Es existieren nach der Expansion also mehr Mikrozustände und das System besitzt eine höhere Entropie. |
Entropie-Formel (wikibooks) erklärt die Formel und den Logarithmus
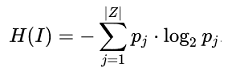
10. Entropie und Entropieströme
Entropie, elektrische Ladung und Impuls sind extensive Größen,
Temperatur, elektrisches Potential und Geschwindigkeit die zugehörigen „energiekonjugierten“ intensiven.
An dieser Gegenüberstellung erkennt man, dass die Entropie für die Wärmelehre so wichtig ist, wie
die elektrische Ladung für die Elektrizitätslehre und der Impuls für die Mechanik.
Und Entropieströme spielen in der Wärmelehre eine ebenso wichtige Rolle wie elektrische Ströme in der Elektrizitätslehre und Kräfte (Impulsströme) in der Mechanik. Es ist daher konsequent, die Wärmelehre mit der Entropie zu beginnen. Wärmelehre ohne Entropie ist nur ein Notbehelf. (Herrmann, KPK:60)
Die Zustandsgröße Entropie als Wärmemass
Die Vorstellung, die Entropie sei eine schwierige Größe, man könne sich nur schwer eine Anschauung von ihr bilden, ist weit verbreitet. Sie trifft sicher zu, wenn man die Entropie auf die Clausiussche Art einführt. Führt man sie statistisch ein, so ist es leichter, sich eine Anschauung von ihr zu bilden, nämlich als Mass für die mikroskopische Unordnung eines Systems. Allerdings ist diese Anschauung für das Lösen praktischer Probleme nicht sehr nützlich.
Wir haben daher einen dritten Weg für die Einführung der Entropie gewählt, einen Weg, der auf Callendar (1911) zurückgeht und von Job (1972) und Falk (1985) ausführlich beschrieben und begründet wurde. Er beruht auf der Einsicht, dass die Eigenschaften der physikalischen Grösse Entropie sehr gut mit den Eigenschaften des umgangssprachlichen Begriffs „Wärme“ oder „Wärmemenge“ übereinstimmen. Diese Übereinstimmung ist so gut, dass man behaupten kann, dass es kaum eine andere physikalische Grösse gibt, für die
wir aus unserer gewöhnlichen Erfahrung eine so gute Anschauung haben.
============
Formel für die verschiedenen Aggregatzustände eines Stoffes mit gleicher Stoffmenge[Bearbeiten]
Festkörper, insbesondere Kristalle, haben eine kleinere Entropie als Flüssigkeiten und Flüssigkeiten eine kleinere als Gase, wenn man denselben Stoff und diesselbe Stoffmenge betrachtet.
SFeststoff < SFlüssigkeit < SGas
Ss < Sl < Sg
wobei s = solid = fest, l = liquid = flüssig, g = gasförmig ist
-->
[ Entropiefluss ]
[ Beispiele ]
[ ]
[ ]
[Systemphysik-Wiki]
[ Arieh Ben-Naim ]
[wp Adiabatische_Erreichbarkeit]
[wp Thermodynamik]